
第三類體外診斷試劑注冊證變更(登記事項變更)服務
依據《體外診斷試劑注冊管理辦法》相關規定,第三類體外診斷試劑實行注冊管理。已注冊的第三類體外診斷試劑,醫療器械注冊證及其附件載明的內容發生變化,注冊人應當向原注冊...
服務價:¥電議
好評系數:

依據《體外診斷試劑注冊管理辦法》相關規定,第三類體外診斷試劑實行注冊管理。已注冊的第三類體外診斷試劑,醫療器械注冊證及其附件載明的內容發生變化,注冊人應當向原注冊部門申請注冊變更,并按照相關要求提交申報資料。登記事項變更資料符合要求的,食品藥品監督管理部門應當在10個工作日內發給醫療器械注冊變更文件。登記事項變更資料不齊全或者不符合形式審查要求的,食品藥品監督管理部門應當一次告知需要補正的全部內容。
未依法辦理注冊登記事項變更有何后果
未依法辦理第三類體外診斷試劑注冊登記事項變更的,由縣級以上人民政府食品藥品監督管理部門責令限期改正;逾期不改正的,向社會公告未備案單位和產品名稱,可以處1萬元以下罰款。其次,應該提早辦理變更登記,以防臨檢仍處于辦理階段出現。
有以下情形的,需辦理注冊證登記事項變更
1、注冊人名稱變更、注冊人住所變更;
2、境內體外診斷試劑生產地址變更;
3、代理人變更、代理人住所變更。
注意:注冊人應在相應的生產許可變更后辦理登記事項變更。
辦理三類IVD注冊證(登記事項變更)所需材料
1、申請表;
2、證明性文件:營業執照和組織機構代碼證;
3、注冊人關于變更情況的聲明;
4、原醫療器械注冊證及其附件的復印件、歷次醫療器械注冊變更文件復印件;
5、關于變更情況相關的申報資料要求:企業名稱變更核準通知書、相應詳細變更情況說明及相應證明文件、應當提供相應變更后的生產許可證。
第三類IVD注冊變更(登記事項變更)服務流程
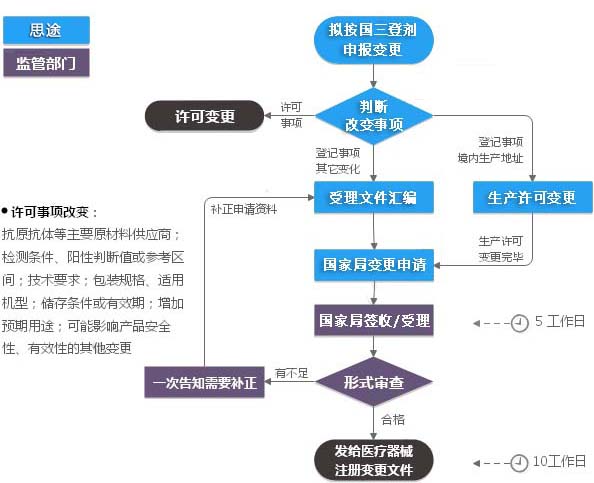
第三類IVD注冊變更(登記事項變更)官方收費標準
辦理三類IVD注冊證登記事項變更,官方不收取變更申請費用。
第三類IVD注冊變更(登記事項變更)服務辦理依據
| 文件名稱 | 文號 |
|---|---|
| 《醫療器械監督管理條例》 | 650號文件 |
| 《體外診斷試劑注冊管理辦法》 | 局令5號 |
| 關于公布體外診斷試劑注冊申報資料要求和批準證明文件格式的公告 | 2014年44號 |
第三類IVD注冊變更(登記事項變更)服務周期
立項階段
預算、合同、考慮期,7個工作日。
受理前資料準備
資料收集、申報資料撰寫、資料確認、蓋章,預計15個工作日。
申請后
登記事項變更法規時間15個工作日,約1個月。
預算合計
立項后至注冊登記變更完成,約2個月。
第三類IVD注冊變更(登記事項變更)推薦服務
| 三類IVD產品注冊服務 | 二類IVD產品注冊服務 |
| IVD臨床試驗服務 | GMP年度輔導服務 |

立即咨詢
 最新文章
最新文章 2025-09-16
2025-09-16 2025-09-16
2025-09-16 2025-09-16
2025-09-16 2025-09-16
2025-09-16 2025-09-16
2025-09-16八年
醫療器械服務經驗
-
多一份參考,總有益處
聯系思途,免費獲得專屬《落地解決方案》及報價
咨詢相關問題或咨詢報價,可以直接與我們聯系
思途CRO——醫療器械注冊臨床第三方平臺
- 在線咨詢
- 在線客服
- 服務熱線
北京公司
186-0382-3911鄭州公司
186-0382-3910合肥公司
188-5696-0331 - 微信咨詢

- 返回頂部











 豫公網安備 41010202003160號
豫公網安備 41010202003160號